

近年、インフルエンザや新型コロナなどの感染症を理解するうえで、「シアル酸糖鎖」の役割が重要視されています。シアル酸は、人体のほぼすべての細胞表面に存在する分子で、免疫調節や自己認識、神経機能などに関わる生命維持に欠かせない存在です。しかしその一方で、多くのウイルスがこのシアル酸を利用して細胞に侵入するという特徴も持っています。
ウイルスは自ら増殖することができず、宿主の細胞に侵入することで増えます。その際、細胞表面の特定の分子に結合する必要があります。この分子は「レセプター」と呼ばれ、ウイルスが強く結合する真のレセプターと、その結合を助けるコレセプターがあります。シアル酸糖鎖は、この両方の役割を担うことができる点が特徴です。
例えば、インフルエンザウイルスでは、シアル酸が真のレセプターとして直接感染に関与します。一方、新型コロナウイルスではACE2という分子が主な受容体ですが、シアル酸はその結合を助けるコレセプターとして働く可能性が示されています。このように、シアル酸はウイルスの種類によって異なる形で感染に関わっています。
シアル酸は、主にα2-3、α2-6、α2-8といった結合様式を持ちます。ウイルスはこの違いを厳密に識別しており、感染する相手や部位を決定しています。例えば、鳥インフルエンザウイルスはα2-3型(鳥型)を、ヒトの季節性インフルエンザウイルスはα2-6型(ヒト型)を利用します。この違いが、感染の広がり方や重症度に大きく関わっています。
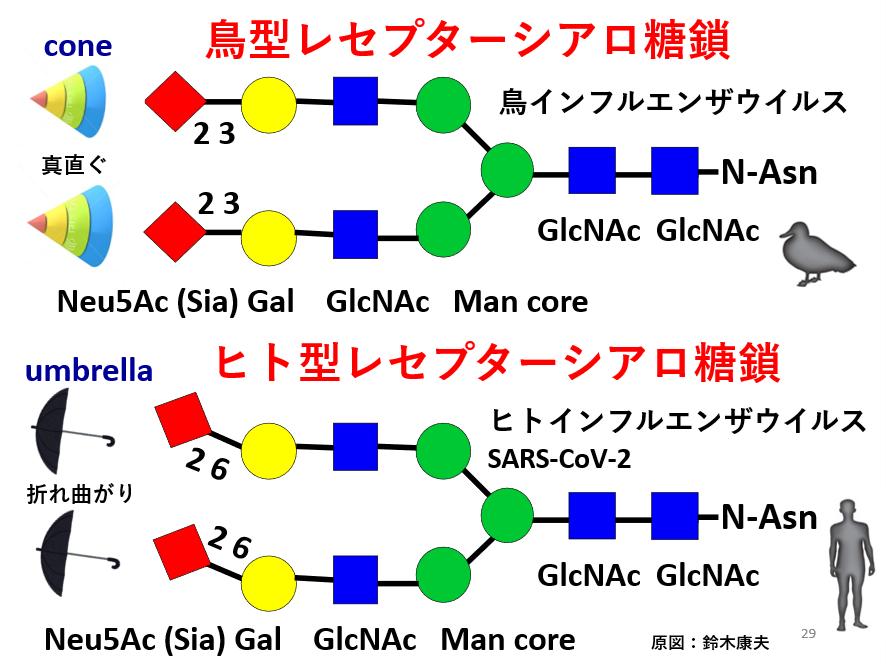
シアル酸の結合様式は、立体構造的に異なっており、鳥型レセプター (2-3Sia) の場合は、真っすぐな円錐型(cone)、ヒト型レセプター (2-6Sia) の場合は折れ曲がった傘型 (umbrella)をしていることが報告されています。
さらに重要なのは、ウイルスが変異によってこの結合性を変えると、新たな宿主へ感染できるようになる可能性がある点です。鳥インフルエンザウイルスがヒト型への結合能力を獲得すると、人から人へ広がるリスクが高まるため、現在も変異の監視が行われています。また一部のウイルスは、糖鎖の種類だけでなく長さや立体構造まで識別する能力を持つことも分かっています。
インフルエンザウイルスには、ヘマグルチニン(HA)とノイラミニダーゼ(NA)という2つの重要なスパイクタンパク質があります。HAはシアル酸に結合して感染を開始し、NAはシアル酸を切断してウイルスの放出を助けます。この働きにより、ウイルスは効率よく感染と拡散を繰り返すことができます。
また、シアル酸を利用するウイルスは非常に多く、ムンプスウイルス、パラインフルエンザウイルス、ジカウイルス、アデノウイルスなど、多くの感染症原因ウイルスがこの仕組みを共有しています。新型コロナウイルスも、ACE2に加えてシアル酸への結合性を獲得したことで、急速な感染拡大につながった可能性が指摘されています。
さらにMERSコロナウイルスでは、別の受容体に加えてα2-3型シアル酸への結合が感染の初期段階を助けると考えられています。動物ではこの型が多く存在するため感染が広がりやすく、一方でヒトでは分布が異なるため、ヒト間感染が限定的になる要因とされています。
このようにシアル酸は、単なる分子ではなく、ウイルス感染の成立と拡大を左右する重要な鍵です。しかも多くのウイルスが共通して利用するため、この部分を標的にした対策は非常に有効と考えられます。
そこで注目されているのが、「疑似シアル酸糖鎖」を用いた感染予防です。これは、ウイルスが結合する前に、シアル酸に似た物質で先に捕まえることで、細胞への侵入を防ぐ戦略です。この方法は、ウイルスの変異に影響されにくく、インフルエンザや新型コロナを含む幅広いウイルス感染症に応用できる可能性があります。
シアル酸は、私たちの体にとって不可欠でありながら、同時にウイルスに利用される「二面性」を持つ分子です。この仕組みを理解することは、感染症の本質を知り、より効果的な予防法を考えるうえで大きなヒントになります。今後は、この共通の感染メカニズムに着目した新しい対策が、ますます重要になっていくと考えられます。
静岡県立大学名誉教授・鈴木康夫




